PIK3CA-Mutationen aus zellfreier DNA
(Liquid Biopsy) zur Therapieentscheidung
beim Mammakarzinom
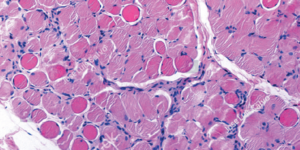
Über 70 % der Mammakarzinome sind HR-positiv und HER2-negativ. Die übliche adjuvante Behandlung ist in diesem Fall die endokrine (antihormonelle) Therapie, die allerdings nicht bei allen Patienten anschlägt. Bei 40 – 50 % dieser HR-positiven/HER2-negativen Patienten mit einem Brustkrebs im fortgeschrittenen oder metastasierten Stadium sind aktivierende PIK3CA-Mutationen im Tumor nachweisbar, die zu einer Hyperaktivierung des PI3K/Akt-Signalweges führen (André et al. 2019, Strohkamp et al. 2021). Dies ist mit einer Stimulierung des Tumorwachstums, einer Resistenzentwicklung gegenüber der Hormontherapie und einer schlechteren Prognose für die Patienten assoziiert. Die Mehrheit der aktivierenden somatischen PIK3CA-Mutationen treten in der Helix- und der Kinase-Domäne auf. Dabei machen vier Hotspot-Mutationen (E542K, E545K, H1047R und H1047L) mehr als 80 % der PIK3CA-Mutationen in Mammakarzinomen aus (Ellis und Ma 2019, Keraite et al. 2020).
Bei durch somatische PIK3CA-Mutationen erworbener Hormonresistenz sollte die Gabe von PIK3-Inhibitoren erwogen werden. Hierfür muss jedoch eine somatische PIK3CA-Mutation im Tumorgewebe bzw. in zirkulierender Tumor-DNA (Liquid Biopsy) nachgewiesen werden. Der PIK3-Inhibitor Alpelisib (Handelsname Piqray®) wird in Kombination mit dem Anti-Östrogen Fulvestrant (Handelsname Faslodex®) zur Behandlung von postmenopausalen Frauen und Männern mit einem HR-positiven, HER2-negativen, lokal fortgeschrittenen oder metastasierten Mammakarzinom mit somatischen PIK3CA-Mutationen angewendet, wenn die Erkrankung nach endokriner Therapie als Monotherapie fortschreitet. In der Phase-III-Studie SOLAR-1 wurde gezeigt, dass die Therapie bei Patienten mit Alpelisib + Fulvestrant zu einer statistisch signifikanten Verlängerung des Progressions-freien Überlebens führte (André et al. 2021). Mit einer im Praxisnetz Humangenetik Deutschland neu etablierten Methode können mittels eines NGS- (Next Generation Sequencing-) Verfahrens diese PIK3CA-Mutationen aus zellfreier DNA (Liquid Biopsy) detektiert werden.
Wo kann die Analyse durchgeführt werden?
Hinweise zur Abrechnung
Diese Untersuchung ist eine Leistung der gesetzlichen Krankenkassen und wird über die GOPen 19462 und 19463 des EBM abgerechnet. Wir benötigen einen Laborüberweisungsschein Muster 10.
Laut der aktuellen Angaben von Novartis wurde Piqray® zum 01.05.2021 vom deutschen Markt zurückgezogen, bleibt jedoch unabhängig davon in der EU zugelassen. Es kann somit weiterhin Patienten in Deutschland verordnet und in Rücksprache mit der jeweiligen Krankenkasse über eine Apotheke aus EU-Ländern (gem. § 73 Abs. 1 AMG) bezogen werden. Mit der Krankenkasse ist zudem die Frage der Kostenübernahme zu klären.
Quellen
- Ellis und Ma. Curr Oncol Rep. 2019 Dec 11;21(12):110
- Keraite et al. Sci Rep. 2020 Oct 13;10(1):17082
- André et al. N Engl J Med. 2019 May 16;380(20):1929-1940
- Strohkamp et al. Journal Onkologie 4/2021
- www.krebsgesellschaft.de
- Interdisziplinäre S3-Leitlinie für die Früherkennung, Diagnostik, Therapie und Nachsorge des Mammakarzinoms (Version 4.4), Juni 2021, Einheitlicher Bewertungsmaßstab (EBM) 202
- www.novartis.de/arzneimittel-produkte/piqray-informationen-zur-risikominimierung.
Autoren:
Dipl.-Biol. Vivien Klaschka, PD Dr. med. Stefan Krüger, MHBA, Dipl.-Mol.Med. Maria Großmann (GP für Humangenetik Dresden), Dr. rer. nat. Beate Küchler, PD Dr. Jens Plaschke (MEWIGEN Dresden)
Magenkarzinome im Rahmen anderer erblicher Tumorsyndrome
Ein erhöhtes Risiko für Magenkarzinome besteht auch im Rahmen anderer erblicher Tumorsyndrome. Insbesonde-reisthierdiehäufigsteFormvonerblichemDarmkrebs (das so genannte HNPCC/Lynch-Syndrom) zu nennen, bei dem die Träger einer ursächlichen genetischen Veränderungen ein erhöhtes Risiko für Darmkrebs, aber auch für Tumoren in der Gebärmutter, den Eierstöcken, dem Magen, dem Dünndarm, der Bauchspeicheldrüse, den ableitenden Harnwegen und für bestimmte Hauttumoren tragen. Auch bei verschiedenen gastrointestinalen Polyposis-Syndromen ist ein erhöhtes Magenkarzinomrisiko beschrieben.
Dies sind vor allem die Familiäre Adenomatöse Polyposis und das verwandte GAPPS (gastric adenocarcinoma and proximal polyposis of the stomach), die durch Mutationen im APC-Gen verursacht werden, sowie die Juvenile Polyposis (SMAD4- und BMPR1A- Gen) und das Peutz-Jeghers-Syndrom (STK11-Gen). Sehr selten liegt auch ein Li-Fraumeni-Syndrom zugrunde, das mit einem erhöhten Risiko für eine Vielzahl von Tumoren einhergeht.
Familiäres Magenkarzinom
Klinik
In vielen Familien, in denen eine Häufung von Magenkarzinomen eine erbliche Ursache vermuten lässt, kann derzeit keine genetische Veränderung nachgewiesen werden. Es ist denkbar, dass in diesen Familien Varianten in bislang nicht bekannten Risikogenen für das familiäre Auftreten von Magenkarzinomen verantwortlich sind. Der Nachweis eines erblichen Tumorsyndroms bei einem Patienten hat weitreichende Konsequenzen für seine weitere klinische Betreuung. Dies gilt zum einen für die Wahl des operativen Verfahrens, bei dem das hohe Risiko für Zweitkarzinome berücksichtigt werden muss. Zum anderen benötigen auch gesunde Träger einer pathogenen CDH1-Mutation lebenslang eine intensivierte Vorsorge bezüglich Magenkarzinomen, bei Frauen zusätzlich bezüglich Mammakarzinomen.
Genetik
Um eine sinnvolle Früherkennung zu gewährleisten sind engmaschige Biopsien der Magen- wand notwendig, da diffuse Magenkarzinome im Frühstadium häufig innerhalb der Magenwand wachsen und endoskopisch nicht zu erkennen sind. Lange wurde von Experten-Netzwerken die prophylaktische Gastrektomie bei gesicherten Mutationsträgern als sinnvollste Maßnahme emp- fohlen. Inzwischen wird diese Empfehlung aufgrund der häufig begleitenden Einschränkung derLebensqualität jedoch wieder vorsichtiger ausgesprochen. (1)
Quellen:
(1.) van der Post RS, Vogelaar IP, Carneiro F, Guilford P, Huntsman D, Hoogerbrugge N, u.a.Hereditary diffuse gastric cancer: updated clinical guidelines with an emphasis on germline CDH1 mutation carriers. J Med Genet. Juni 2015;52(6):361–74.
Klinik
Beim Hereditären Paragangliom-Phäochromozytom-Syndrom besteht neben der Neigung zu Paragangliomen ein erhöhtes Risiko für Phäochromozytome.
Paragangliome und Phäochromozytome treten z. B. auch bei Patienten mit Von-Hippel-Lindau-Syndrom (Mutationen im VHL-Gen) oder Neurofi- bromatose Typ 1 (Mutationen im NF1-Gen) auf.
Genetik
Bei 20 – 70 % der familiären Fälle werden Mutationen in den Genen SDHD, SDHB oder SDHC nachgewiesen. Seltener werden Mutationen in den Genen SDHAF2, SDHA, MAX und TMEM127 gefunden. Für weitere Gene (z. B. KIF1B und EGLN1) ist ein Zusammenhang bisher nicht gesichert.
Weitere Formen
Endokrine Tumore sind u. a. auch im Rahmen folgender weiterer Erkrankungen beschrieben: Tumore der Nebennierenrinde (adrenokortikale Karzinome) beim Li-Fraumeni-Syndrom (TP53-Mutationen), Hyperparathyreoidismus bei Mutationen in den Genen CASR oder CDC73, Hypophy- sentumore bei Mutationen in den Genen AIP oder PRKAR1A.
Handlungsempfehlungen
Aufgrund des erhöhten Tumorrisikos vieler der o. g. Erkrankungen werden für Mutationsträger teilweise spezielle Früherkennungsuntersuchungen und ggf. prophylaktische Operationen empfohlen.
Quellen: Ferreira et al. Cancer Manag Res. 2013 May 8;5:57-66, Khatami and Tavangar Biomark Insights 2018 Jul 2;13, Martucci and Pacak Curr Probl Cancer. 2014 Jan-Feb;38(1), Norton et al. Surg Oncol Clin N Am. 2015 Oct;24(4) Thakker et al. Clinical Practice. J Clin Endocrinol Metab, 2012, 97(9):2990-3011, Gene- Reviews, OMIM